電子カルテと治験データ収集システムとの高度なデータ連携に向けた共同研究を実施
~医療機関における転記作業時間、製薬企業におけるSDV時間を削減~
報道発表
2024年6月11日
国立研究開発法人国立がん研究センター
中外製薬株式会社
株式会社NTTデータ
発表のポイント
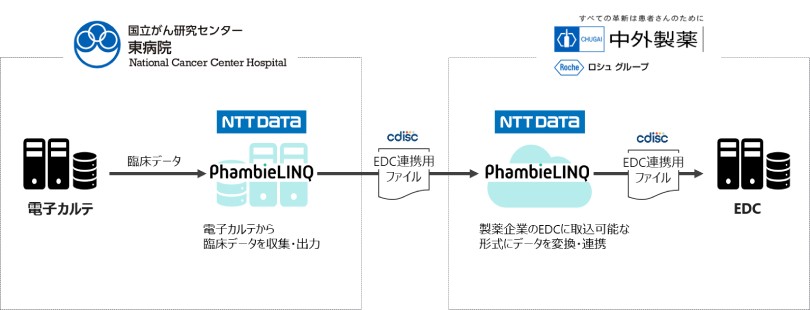
- PhambieLINQ®を活用して、患者背景やバイタルサイン、臨床検査値に加えて、有害事象並びに併用薬といった臨床データを電子カルテからEDCへ連携できることが確認されました。
- データ連携によって、医療機関においては電子カルテからEDCへの転記作業時間や製薬企業からのクエリ(問合せ)数が削減し、製薬企業においてはSDV作業時間の削減が確認されました。
- 本研究のような治験業務のデジタル化を前進させる取り組みによって、これまでの品質を維持しながら治験業務の更なる効率化が進み、一日も早く患者さんに新しい医薬品が届くようになることが期待されます。
概要
国立研究開発法人国立がん研究センター(東京都中央区、理事長:中釜 斉)東病院(千葉県柏市、病院長:土井 俊彦、以下:国立がん研究センター東病院)、中外製薬株式会社(本社:東京都中央区、代表取締役社長 CEO:奥田 修、以下:中外製薬)と株式会社NTTデータ(本社:東京都江東区、代表取締役社長:佐々木 裕、以下:NTTデータ)は、電子カルテに記載された臨床データのEDC注1への連携に関する共同研究を実施しました。
電子カルテに記録された臨床データを製薬企業のEDCに連携する取り組みは従前より広く行われていましたが、連携対象の臨床データは限定的で、データ連携の拡充が求められていました。本研究では、PhambieLINQ®注2を活用し、疾患領域を限定せず、有害事象・併用薬を含めて、治験で必要となる主要な臨床データの連携が可能となりました。今回の結果は世界的に見ても先進的な事例であり、治験業務のデジタル化を前進させるものです。
三者は今後、本共同研究の結果を活用し、医療機関・製薬企業の治験業務効率化・高品質化を実現し、新しい医薬品が1日でも早く患者さんに届くように貢献していきます。
背景
新薬開発は、研究、治験での臨床データの収集・解析、有効性と安全性の評価などのプロセスを経て平均で9~17年程度注3かかり、製薬企業と医療機関の双方で多くの労力・時間が費やされる臨床データの収集においては、業務効率化と品質確保の両面が課題となっています。
近年、医療機関の電子カルテから製薬企業のEDCに臨床データを電子的に連携させる取り組みが注目を集めています。しかしながら、電子カルテとEDCの互換性や製品間の差異等のため業界全体での普及は進んでおりません。中でも、患者さんの安全性評価で重要となる有害事象や併用薬情報については、データ連携の取り組みは極めて稀です。
NTTデータは、どの医療機関や製薬企業でも、電子カルテとEDCのデータ連携を可能とする治験DXサービス「PhambieLINQ®」の開発および提供を進めています。現在PhambieLINQ®において連携可能な臨床データは、患者背景、臨床検査値、バイタルサインの3種類ですが、電子カルテには、その他にも有害事象や併用薬等の情報も記録されています。これらがEDCへ電子的に連携可能となれば治験業務のさらなる効率化につながることが期待されます。
国立がん研究センター東病院は、医療DXの加速に向け、デジタル技術を活用したデータの収集や利活用に向けた構造化等のデータ整備、治験業務改革を進めています。中外製薬は、「CHUGAI DIGITAL VISION 2030」の基本戦略の1つにバリューチェーンの効率化を掲げ、治験プロセスのさらなる加速を目指しています。中外製薬とPhambieLINQ®を利用する国立がん研究センター東病院は、NTTデータとともに、有害事象・併用薬を含む、疾患に関わらず試験共通で必要となる主な臨床データをEDCへ連携する共同研究を実施しました。
共同研究について
| 目的 | 電子カルテ等に記録された有害事象・併用薬を含む臨床データを治験へ利活用(症例データ報告・収集の効率化)するにあたっての技術的、運用上の課題解決 |
|---|---|
| 研究内容 |
|
| 期間 | 2023年6月から2024年1月まで |
| 検証結果 |
|
今後について
国立がん研究センター東病院、中外製薬、NTTデータは、今回の検証結果を踏まえ、実試験での有害事象・併用薬を含むデータ連携を目指します。
今回実現した高度なデータ連携は、他医療機関及び他製薬企業を含めた業界全体の治験業務効率化・高品質化の実現につながるものです。データ連携に必要なシステムの整備・普及を進めるためにも、各医療機関が有害事象・併用薬を含む臨床データを構造的に記録・管理することや、臨床データの収集形式を製薬企業間で標準化・最適化することなど、業界全体での連携・協力が不可欠です。
国立がん研究センター東病院、中外製薬、NTTデータは、新しい医薬品が患者さんに1日でも早く届く世界の実現に向け、今回の検証結果を踏まえた業界全体への働きかけを協働して実施していくなどして、また複雑化・拡大する治験業界における人材不足を補う上での各業界のスタッフの業務の効率化を通じ、新薬開発の効率化と最適な品質につながる仕組みづくりに貢献していきます。
各社コメント
本共同研究によって医療機関、依頼者双方の業務改善効果の可能性が示唆されたことは大変素晴らしいことだと思います。日本の治験環境改善のため、また、世界から後れを取らないためにも三者が協力し合って推し進めることが重要です。また、昨今の課題である我が国のドラッグラグ・ロスの要因の一つとして治験コストの問題があり、このような取り組みや、当院で先進的に取り組むR-SDV注5などを活用しながら、モニタリング費用を抑えることも将来可能ではないかと考えています。一方で、データ連携は導入に際し、条件やコスト面から実装可能な施設が限られるため、システムの普及をどこまで進めるかは議論の余地が残ります。治験実施施設として業務効率化を推進しながら必要な質を担保し、私たちの最終目標である患者に薬を届ける最適な方法は何かを考え、引き続き取り組んでまいります。
国立がん研究センター東病院 臨床研究支援部門 研究実施管理部長 久保木 恭利
新たな医薬品を患者さんに一日でも早くお届けできるために、品質が担保された治験データを安全かつ効率的に収集することは製薬業界共通の課題です。中外製薬は「CHUGAI DIGITAL VISION 2030」の基本戦略の1つとしてバリューチェーンの効率化を掲げ、治験プロセスのさらなる加速を目指しています。デジタル技術を活用し、医療機関・製薬企業共通の治験プラットフォームの構築を目指す取り組みに、当社のこれまでの知見や経験を活かすことができ大変嬉しく思います。
中外製薬株式会社 参与 デジタルトランスフォーメーションユニット長 鈴木 貴雄
国立がん研究センター東病院様、中外製薬様とともに、世界的に見ても先進的なテーマで治験業務のデジタル化に関する共同研究を完遂できましたこと、大変嬉しく思います。NTTデータはデジタルヘルスケアのビジョン注6に基づき、志を同じくするお客様、共創パートナーとともに、ヘルスケア領域における社会課題をデジタル化で解決すべく取り組みを加速させているところです。今回の共同研究を通じて得られた知見を活かして治験業務の効率化・高品質化に貢献するとともに、持続的に誰もが平等に質の高い医療サービスが受けられる社会、安心安全な暮らしができる健康長寿社会の実現を目指して取り組んでまいります。
株式会社NTTデータ 執行役員 第二公共事業本部長 青木 千恵
注釈
-
注1
EDC(Electronic Data Capture)
臨床データを電子的に収集する仕組み、もしくはそのシステムのことです。 -
注2
PhambieLINQ®
NTTデータが開発した、医療機関と製薬企業をつなぐ治験総合プラットフォームです。医療機関と製薬企業のデータ連携を実現し、データの高品質化、治験プロセスの効率化に寄与します。
「PhambieLINQ®」は日本国内における株式会社NTTデータの商標です。https://phambielinq.com/ -
注3
出典:日本製薬工業協会.「薬の情報Q&A」
https://www.jpma.or.jp/about_medicine/guide/med_qa/q33.html(参照 2024年5月) -
注4
SDV(Source Data Verification)
倫理的及び科学的な治験の適切な実施及びデータの信頼性等を検証する作業のことです。 -
注5
R(Remote)-SDV
医療機関外から、システムを用いて原資料(正確な複写であることが検証によって保証された複写物又は転写物を含む)を閲覧しSDVすることです。 -
注6
NTTデータのデジタルヘルスケアのビジョン
NTTデータは「Harmonized Well-being with Data~生活に溶け込む健康づくりが進む未来~」を描いたデジタルヘルスケアに関するホワイトペーパーを公開しています。
https://www.nttdata.com/jp/ja/industries/healthcare/
- 商品名、会社名、団体名は、各社の商標または登録商標です。
お問い合わせ先
国立研究開発法人国立がん研究センター
報道関係者の皆様
企画戦略局
広報企画室(柏キャンパス)
TEL:04-7133-1111(代表)
E-mail:ncc-admin@ncc.go.jp
中外製薬株式会社
報道関係者の皆様
広報IR部
メディアリレーションズグループ
TEL:03-3273-0881
E-mail:pr@chugai-pharm.co.jp
投資家の皆様
広報IR部
インベスターリレーションズグループ
TEL:03-3273-0554
E-mail:ir@chugai-pharm.co.jp
株式会社NTTデータ
報道関係者の皆様
広報部
西原
E-mail:nttdata-pr-inquiries@am.nttdata.co.jp
本共同研究・ソリューション関連
第二公共事業本部
デジタルウェルフェア事業部
星野
E-mail:phambielinq-sales@am.nttdata.co.jp
国立研究開発法人国立がん研究センター東病院について
国⽴がん研究センター東病院では、すべての患者さんに世界レベルのがん医療を提供するため、様々な職種からなる「多職種チーム」で患者さんにとってベストの治療を選択し、きめ細かなサポートを⾏っています。ロボット⽀援⼿術や陽⼦線をはじめ、最新の医療機器を有し、内視鏡治療や体への負担が少ない低侵襲⼿術、また、薬物療法や数多くの治験に取り組んでいます。
URL:https://www.ncc.go.jp/jp/ncce/index.html
中外製薬株式会社について
中外製薬(本社:東京)は、抗体エンジニアリング技術をはじめとする独自の創薬技術基盤を強みとする、研究開発型の製薬企業です。ロシュ・グループの重要なメンバーであるとともに、東京証券取引所プライム市場の上場企業として、自主独立経営の下、アンメットメディカルニーズを満たす革新的な医薬品の創製に取り組んでいます。中外製薬に関するさらに詳しい情報はhttps://www.chugai-pharm.co.jp/をご覧下さい。
株式会社NTTデータについて
NTTデータは、豊かで調和のとれた社会づくりを目指し、世界50カ国以上でITサービスを提供しています。デジタル技術を活用したビジネス変革や社会課題の解決に向けて、お客さまとともに未来を見つめ、コンサルティングからシステムづくり、システムの運用に至るまで、さまざまなサービスを提供します。
URL:https://www.nttdata.com/jp/ja/
